Sie helfen, wenn kein Antibiotikum mehr wirkt
Resistente Supererreger sind auf dem Vormarsch. Expert:innen sprechen bereits von einer »stillen Pandemie«, die pro Jahr über eine Million Menschenleben kostet. Doch in Europa wird an einer neuen Therapie geforscht, die multiresistente Keime zerstören kann. Ein Bericht, wie weit die Wunderwaffe ist.
Ein kleiner Schnitt in den Finger, ein unbedachter Schluck Wasser, ein Happen des ungekühlten Mittagessens vom Vortag. Es sind Kleinigkeiten wie diese, die vor kaum mehr als 100 Jahren noch ein Todesurteil sein konnten.
Zu dieser Zeit zählten von unsichtbaren Erregern ausgelöste Infektionen zu den gefürchtetsten Killern überhaupt. Auch lebensgefährliche Krankheiten wie Lungenentzündung, Tuberkulose oder Syphilis grassierten. Selbst in den »entwickelten« Industrieländern betrug die durchschnittliche Lebenserwartung
Erst im Jahr 1928 kommt es zu einer der wohl größten medizinischen Revolutionen. Der britische Mediziner Alexander Fleming entdeckt die bakterientötende Wirkung von Penicillin. Spätestens als das neue Medikament mit Ende des Zweiten Weltkrieges allgemein verfügbar wird, beginnt die »goldene Ära« der Antibiotika, die künftig Millionen von Leben retten sollen.
Antibiotika gelten seither als eine Art Superwaffe. Für eine Weile sah es ganz danach aus, als könnten sie die meisten bakteriellen Krankheiten in den reichen Ländern des
In den letzten Jahren mehren sich jedoch Stimmen, die vor dem Ende dieser Ära warnen. Sogar von einer »stillen Pandemie« ist die Rede, die im Schatten des Coronavirus pro Jahr mindestens 1,3 Millionen Menschen das Leben kostet. Immer neue Bakterien treten auf den Plan, die immun geworden sind gegen die einstige Superwaffe.

Wer sich mit einem solchen resistenten Erreger ansteckt, zum Beispiel nach einer Operation im Krankenhaus, hat nur wenig Aussicht auf Genesung. Die Supererreger können dafür sorgen, dass chronisch infizierte Wunden nicht heilen, oder die Lunge befallen, wo sie Entzündungen auslösen und im schlimmsten Fall zum Tod führen können.
Durch den massenhaften und unüberlegten Einsatz von Antibiotika werden mehr und mehr Erreger resistent gegen einzelne Wirkstoffe. Mehr noch: Einige von ihnen sind bereits »multiresistent« und damit durch gleich mehrere Antibiotikaklassen nicht mehr zu bekämpfen.
Stehen wir am Anfang vom Ende des Antibiotikazeitalters?
Ungeahnte Verbündete
Die Weltgesundheitsorganisation (WHO) zeigt sich
Die Antibiotika-Resistenz ist eine globale Bedrohung, sowohl für die öffentliche Gesundheit als auch für die Wirtschaft.
Doch trotz all der gerechtfertigten Warnungen gibt es auch gute Nachrichten: Das Problem rückt – wenn auch verzögert durch die Coronapandemie – zunehmend auf die globale Agenda von Forschenden auf der ganzen Welt.
Einer der vielversprechendsten Ansätze ist eine lang vergessene Therapieform aus der ehemaligen Sowjetunion, die komplett ohne klassische Antibiotika auskommt. Sie setzt ausgerechnet auf Organismen, die uns die letzten 3 Jahre in Atem hielten: Viren. Eine Gruppe spezieller Viren, die sogenannten Bakteriophagen, befällt und tötet ausschließlich Bakterien, Körperzellen lässt sie in Ruhe.

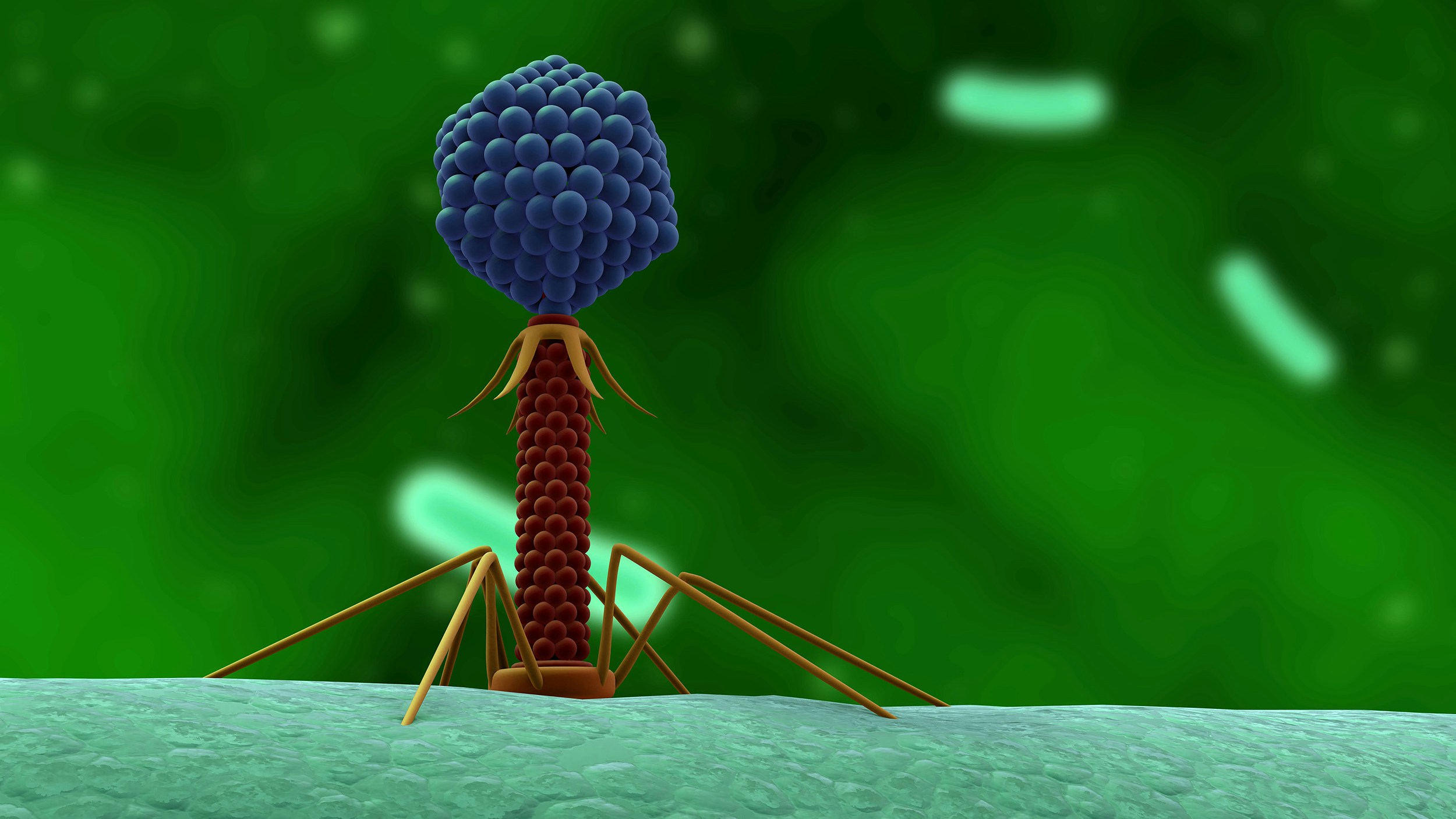
Ein Phage sieht aus, als wäre er der Fantasie einer Science-Fiction-Autorin entsprungen. Eine Art würfelförmiger Kopf, der die Erbinformationen des Virus enthält; ein Körper, der an eine Wirbelsäule erinnert; beinartige Fäden, die zur Fortbewegung genutzt werden.
Können uns diese Viren helfen, im uralten Kampf gegen Bakterien wieder die Oberhand zu gewinnen?
Viren als Heilmittel
Der Gedanke, bei der Bekämpfung einer bakteriellen Infektion ausgerechnet auf Viren zu setzen, erscheint auf den ersten Blick wenig verlockend. Schließlich lernen wir von klein auf, dass Viren gefährliche Krankheiten wie Herpes, Grippe, Covid-19 oder AIDS auslösen.
Bei Bakteriophagen liegen die Dinge anders. Einen Bogen um sie zu machen, ist nicht möglich, immerhin sind sie die zahlenmäßig häufigsten »Wesen« auf der Erde – und trotzdem den meisten Menschen unbekannt. Sie sind überall: in unserer Umwelt, auf unseren Körpern und vor allem in unseren Abwässern, wo sie es auf Bakterien abgesehen haben, die unsere Fäkalien zersetzen. Daher werden sie umgangssprachlich oft als »Bakterienfresser« bezeichnet.
In der Praxis funktioniert das so: Haben Phagen den passenden Wirt gefunden, docken sie mithilfe ihrer Greifarme an (1), bohren die Zellwand auf und injizieren ihre DNA in die Zelle (2). Das gekaperte Bakterium stellt jetzt selbst Phagen her (3), bis seine Hülle zerstört wird und es eine Armada neuer Phagen auf ihren Beutezug entlässt (4). Vermehren sich die krank machenden Bakterien noch weiter, wächst die Phagenpopulation mit. Sind alle Bakterien getötet, verschwinden ihre Jäger mit ihnen, da sie keine Wirte mehr finden, um sich selbst zu reproduzieren.
Einzelne Bakteriophagen-Stämme sind nämlich hochspezialisiert und greifen stets nur eine ganz bestimmte Art Bakterium an – ein Umstand, der für den therapeutischen Einsatz von Phagen essenziell wichtig ist.




Eine vergessene Arznei, bewahrt in Georgien
Entdeckt wurden Phagen bereits 1917 durch den kanadischen Biologen Félix Hubert d’Hérelle, also noch bevor Alexander Fleming die Wirkung von Penicillin nachwies. Dementsprechend enthusiastisch wurde d’Hérelles Entdeckung gefeiert: Es kam zu einem regelrechten Phagenboom in Europa und den USA. Pharmaunternehmen brachten Phagenpräparate auf den Markt, die etwa erfolgreich im Kampf gegen die gefürchtete Ruhr eingesetzt
Doch mit dem Beginn der industriellen Produktion von Penicillin im Jahr 1942 fand diese kurze Blütezeit ein jähes Ende. Die Ära des Antibiotikums hatte begonnen. Mit dieser sehr wirksamen und günstig zu produzierenden neuen Arznei schwand das Interesse an den Phagen in der westlichen Welt rasant, die Forschungsgelder wurden zusammengestrichen.
Nicht so aber in der ehemaligen Sowjetunion: Während des Kalten Krieges waren Antibiotika dort ein
Doch als die Sowjetunion 1991 zerfiel, brach die vormals großzügige Finanzierung des Kremls für die Phagentherapie weg. Der georgische Bürgerkrieg in den Jahren
»Zu Sowjetzeiten wurde jeder – ob Groß oder Klein – erfolgreich mit Phagen behandelt, entweder mit Tabletten oder per intravenöser Injektion«, berichtete mir die medizinische Mikrobiologin Zemphira Alavidze vom Phage Therapy Center in der georgischen Hauptstadt Tiflis, als ich vor fast 5 Jahren zum ersten Mal über die Phagen recherchierte.
Den ersten Artikel zum Thema vom 19. Februar 2018 findest du hier:
In Deutschland wurden die Phagen zu Therapiezwecken zu dieser Zeit gerade erst wiederentdeckt; die Forschung steckte hier bis vor wenigen Jahren noch in den Kinderschuhen. Das erste Projekt namens Phage4Cure (frei übersetzen lässt sich der Name mit »Phagen zum Heilen«) hatte gerade erst begonnen und war vom Bundesministerium für Bildung und Forschung (BMBF) mit 4 Millionen Euro ausgestattet worden.
Was hat sich seither getan?
Der lange Weg zur medizinischen Zulassung
»Wir haben sehr viel von den georgischen Kolleg:innen gelernt, die ihr breites Know-how bereitwillig mit uns geteilt haben«, berichtet die Mikrobiologin Christine Rohde, die bei der Deutschen Sammlung von Mikroorganismen und Zellkulturen am Leibniz-Institut in Braunschweig seit über 30 Jahren an Bakteriophagen forscht und maßgeblich an Phage4Cure beteiligt ist. »Es geht definitiv voran. Wir haben in Deutschland neben Phage4Cure inzwischen weitere finanzschwere, öffentlich geförderte Projekte und auch auf europäischer Ebene tut sich einiges.«

Das Projekt Phage4Cure selbst geht Anfang 2023 in die erste klinische Testphase. Darin werden nach einer langen Zeit der Grundlagenforschung erstmals Patient:innen im Rahmen einer deutschen Studie mit Phagen behandelt. Hier wird getestet, ob Patient:innen mit Mukoviszidose, einer chronischen Lungenerkrankung, von einer Phagentherapie per Inhalation profitieren. Heilen können die Phagen die erblich bedingte Krankheit zwar nicht; sie sollen jedoch das Bakterium Pseudomonas aeruginosa töten, das bei den Betroffenen häufig in der Lunge angesiedelt und resistent gegen Antibiotika ist. Bereits im späten Frühling des nächsten Jahres sollen erste Daten vorliegen.
Pseudomonas aeruginosa
Pseudomonas aeruginosa ist ein sehr widerstandsfähiges Bakterium, das gegen viele Antibiotika resistent ist. Es ist in feuchteren Bereichen von Kliniken zu finden und gehört zu den in Deutschland am meisten auftretenden Krankenhauskeimen. Pseudomonas aeruginosa ist eine der häufigsten Ursachen von nosokomialen Infektionen, wie Harnwegsinfekten oder Lungenentzündungen. Letztere können insbesondere bei immunsupprimierten und AIDS-Patienten schwerwiegende Folgen haben.
Christine Rohde ist zuversichtlich, dass die Studie erfolgreich verläuft. Rückendeckung erhalten sie und ihr Team dabei vom Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), das für die Zulassung von Medikamenten in Deutschland zuständig ist. »Die Patientenkohorten müssen bei dieser Studie nicht so groß sein wie etwa bei der Zulassung von Impfstoffen. Das liegt daran, dass das BfArM aus zahlreichen Einzelfallbehandlungen mit einer langen Historie weiß, dass Phagen sicher sind. Es gibt keine bekannten Nebenwirkungen, solange die Präparate pharmazeutisch gut geprüft und aufgereinigt sind«, sagt Rohde. Im Jahr 2015 hatte eine große internationale Phagen-Expert:innengruppe Qualitätsstandards definiert und publiziert, die Frage ist also kein Neuland.
»Aufgereinigt« bedeutet, dass sichergestellt ist, dass sich nur genau die Phagenstämme in einer Arznei befinden, die medizinisch geboten sind, um einen ganz bestimmten Erreger anzugreifen. Geht alles gut, stehen im kommenden Jahr wissenschaftlich belastbare Daten nach westlichen Standards bereit, um die Phagentherapie in Deutschland und Europa weiter voranzubringen. Phage4Cure dürfte also einen erheblichen Schub leisten.
Phagentherapie in der Praxis
Das 2019 gestartete Projekt
Ziel ist es, eine Sammlung von effektiv wirkenden Phagenpräparaten gegen besonders häufig auftretende multiresistente Bakterienarten aufzubauen, etwa gegen den berüchtigten multiresistenten Krankenhauskeim
Wir wollen zeigen, dass wir in der Lage sind, innerhalb […] von bis zu 2 Wochen eine Phagentherapie für Patienten herzustellen. Wir müssen in diesem Zeitraum die für die Infektion verantwortlichen bakteriellen Krankheitserreger identifizieren, wirksame Bakteriophagen aus einem im Krankenhaus verfügbaren Set verschiedener Phagen auswählen und mit der Therapie beginnen.
Inzwischen wurden die ersten Patient:innen mit den Phagen behandelt. Unter ihnen befinden sich auch ukrainische Soldaten, die bei Kämpfen im Osten des Landes verwundet wurden und unter nicht heilenden, chronischen Wunden leiden, die mit multiresistenten Keimen
Neben dem Bundeswehrkrankenhaus in Berlin arbeitet aktuell vor allem das
In diesem kurzen Video berichten die Mediziner:innen des Nationalen Phagenzentrums der Medizinischen Hochschule Hannover von ihren positiven Erfahrungen mit der Phagentherapie:
Warum die Pharmaindustrie nicht in Phagen investiert
Auch in vielen anderen Staaten in Europa und in den USA erfahren Phagen wieder mehr Aufmerksamkeit. »Das Ganze ist im Moment extrem populär in Europa«, bestätigt Dirk Bumann, stellvertretender Direktor des Nationalen Forschungsschwerpunkts »Neue Ansätze zur Bekämpfung Antibiotika-resistenter Bakterien« in Basel. Im Rahmen einer Podiumsdiskussion des Science Media Centers zum Thema Antibiotikaresistenzen und Alternativen schätzt er das Potenzial der Phagen so ein: »Es gibt zurzeit einige Start-up-Unternehmen, die diesen Ansatz verfolgen, etwa an einem
Doch trotz der vielversprechenden Projekte in ganz Europa gibt es ein zentrales Problem, das den großen Durchbruch der Phagen erschwert: Mit ihnen lässt sich nur schwer Geld verdienen. Da die »Bakterienfresser« frei in der Natur vorkommen und als Grenzgänger zwischen lebendig und tot zumindest eine Art Lebewesen sind, lassen sich einzelne Phagenstämme nicht ohne Weiteres für den medizinischen Einsatz patentieren. Daher schrecken Pharmaunternehmen bisher davor zurück, Geld in die Hand zu nehmen, um aus Phagen Medikamente zu entwickeln, da sie diese am Ende möglicherweise nicht patentieren und
Phagen: Grenzgänger zwischen lebendig und tot
Wie alle Viren sind Phagen im Gegensatz zu Bakterien streng genommen keine Lebewesen. Dazu fehlen ihnen ein eigener Stoffwechsel und die Fähigkeit, sich selbst zu vermehren. Für Letzteres brauchen Viren einen Wirt, in den sie ihr Erbgut einschleusen. Die Wirtszelle wird so gezwungen, den Erreger zu reproduzieren. Wirte können Menschen oder Tiere sein – oder wie im Fall der Phagen eben Bakterien.
Im Rahmen der Profitlogik unseres Wirtschaftssystems, das auch die medizinische Forschung bestimmt, müssen sie aber Profit machen. Die Entwicklung neuer Arzneimittel ist allgemeinhin ein langwieriger, riskanter und teurer Prozess. Schätzungen zu notwendigen Investitionen für ein gänzlich neues Medikament reichen laut einer aktuellen Studie
Schafft es ein neues Medikament dann bis zur Marktreife, muss es diese Kosten wieder einspielen – und zusätzlich Renditen für Investor:innen erwirtschaften. Solange sich an diesem System nichts ändert und gleichzeitig unklar bleibt, ob Phagenpräparate patentiert und im umfangreichen Stil vermarktet werden können, sind groß angelegte Investitionen zurzeit eher unwahrscheinlich.
Hier erkläre ich, wie die Pharmaindustrie mit überteuerten Medikamenten Milliardengewinne einfährt:
Dabei hält Christine Rohde dieses Problem durchaus für lösbar. Denkbar sei es etwa, bestimmte Zusammenstellungen von Phagen in Cocktails oder auch eine bestimmte Darreichungsform wie etwa per Inhalator schützen zu lassen. »Eigentlich müssten die Pharmaindustrie und noch mehr innovative Start-ups endlich erkennen, dass es hier eine Marktlücke gibt, und in die Forschung und Produktion einsteigen.« Das politische Signal, das von der öffentlichen Förderung der Phagenprojekte ausgehe, helfe dabei, die Therapie für Investor:innen nach und nach interessanter zu machen.
Eine Zukunft ohne Phagentherapie können wir uns nicht leisten
Angesichts zunehmender Antibiotikaresistenzen und Hunderttausender Todesopfer pro Jahr sind neue Entwicklungen, die auch gegen resistente Keime eine Chance haben, dringend notwendig. Der Präsident der Bundesärztekammer, Klaus Reinhard, forderte vor diesem Hintergrund erst kürzlich einen »New Deal für die Entwicklung neuartiger Antibiotika«, der neue Anreize für Investitionen schaffen müsse.
In den vergangenen Jahren hätten sich auch in diesem Bereich mehrere große Pharmaunternehmen aus der Entwicklung
Im Kampf gegen multiresistente Keime brauchen wir jeden Verbündeten, den wir kriegen können
Die Phagentherapie bietet enormes Potenzial: Einerseits, um künftig irgendwann Antibiotika einsparen zu können, wenn es Präparate bis zur Marktreife schaffen. Andererseits als »Geheimwaffe«, um schon heute Patient:innen zu helfen, die auf die heutigen Wirkstoffe nicht mehr ansprechen.
Es wäre fatal, weiterhin in erster Linie auf Antibiotika zu setzen – schließlich hat ihr massenhafter und unüberlegter Einsatz in den letzten Jahrzehnten die »stille Pandemie« erst möglich gemacht. Im evolutionären Wettlauf gegen resistente Bakterien können wir Menschen daher jetzt jeden Verbündeten brauchen – selbst wenn es sich dabei um (die richtigen) Viren handelt.
Titelbild: depositphotos - CC0 1.0